Tra i cento composti chimici più importanti l'acido formico è l'acido organico più semplice ma allo stesso tempo più forte, fatto che offre notevoli vantaggi per l'industria chimica. È più ecologico, non corrosivo, facilmente biodegradabile rispetto ad altri acidi organici e inorganici e trova ampia applicazione nell'agricoltura, nell'industria della gomma, in quella farmaceutica, nell'alimentazione animale, nelle concerie e nell'industria tessile. Inoltre, è un riducente di uso frequente, un solvente verde, nonché un elemento costitutivo in varie sintesi chimiche.
Nel 2019 il mercato globale annuo approssimativo dell'acido formico è arrivato a circa 620 milioni di dollari, cifra che manterrà un aumento costante in futuro. L'acido formico non è solo un importante prodotto chimico, è anche un vettore energetico chiave che può fornire soluzioni alla crisi energetica e contribuire alla creazione di strutture di energia rinnovabile. Può produrre direttamente o essere trasformato in una varietà di combustibili di alta qualità tra cui idrogeno (H2), monossido di carbonio (CO), metanolo e bio-oli. In particolare, l'acido formico è considerato uno dei materiali di stoccaggio dell'H2 più promettenti, come vedremo nel dettaglio in questo articolo.
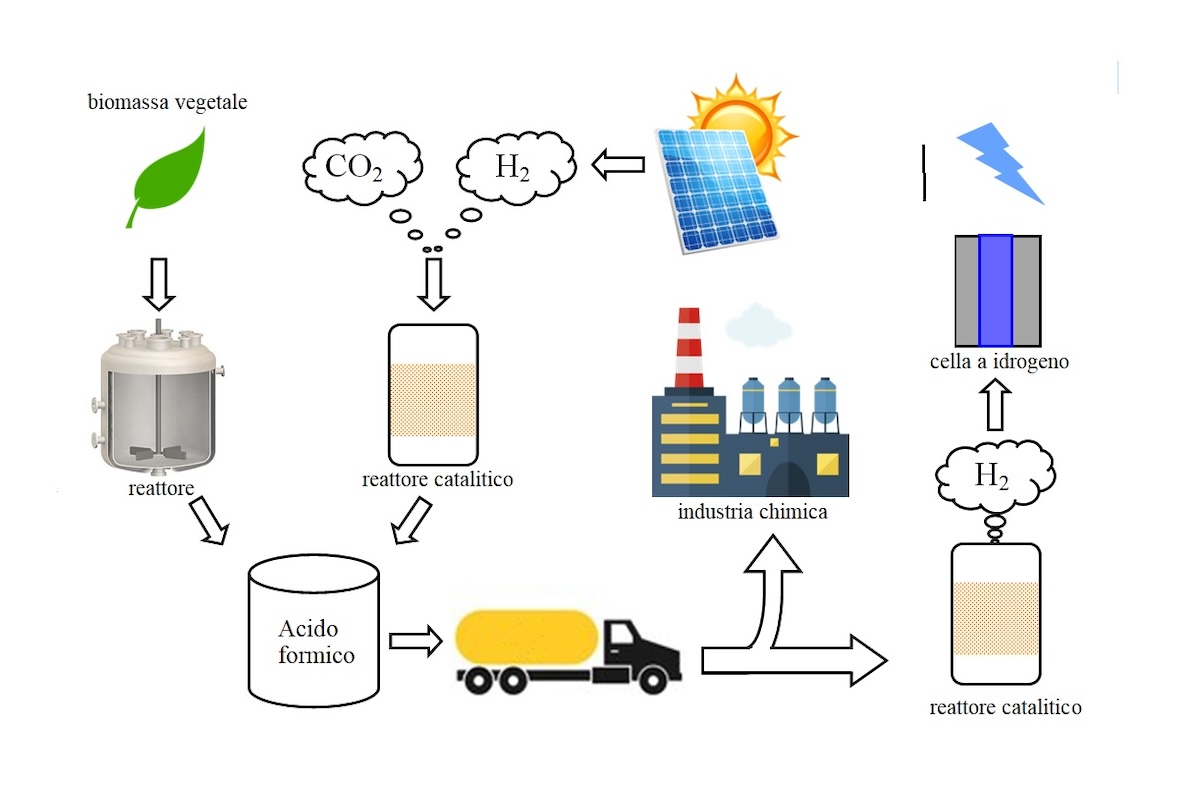
L'acido formico è presente naturalmente nella maggior parte delle formiche, in alcune specie di api e nell'atmosfera a causa delle emissioni delle foreste. Il nome "formico" deriva appunto dal latino formica perché è stato isolato inizialmente mediante distillazione delle formiche. L'attuale produzione industriale di acido formico prevede un metodo in due fasi (1).
Si parte dal metanolo, che a sua volta è prodotto dal gas naturale o dal carbone. Pertanto, l'acido formico attualmente in commercio è a tutti gli effetti un derivato dai combustibili fossili e perciò insostenibile. Tuttavia, la produzione su larga scala di acido formico da risorse rinnovabili è preferibile per mitigare le emissioni di carbonio e combattere il riscaldamento globale. Finora la ricerca ha concentrato i suoi sforzi sullo sviluppo di soluzioni tecnologiche per ottenere acido formico da risorse rinnovabili, principalmente dalla biomassa e dalla CO2.
L'acido formico come vettore energetico
Il principale vantaggio e la potenziale applicazione energetica dell'acido formico sono relativi al suo ruolo di stoccaggio di H2. Il fattore che finora ha limitato di più l'utilizzo dell'idrogeno come vettore energetico al posto del gas naturale o degli idrocarburi è la sua bassissima densità energetica.
Leggi anche Idrogeno da biometano, biometano da idrogeno
La formula chimica dell'acido formico è CO2H2 ed è liquido a temperatura ambiente, questo significa che 46 grammi contengono 2 grammi di H2, ovvero il 4,6%. La densità dell'acido formico è 1,22 chilogrammi/dm3, quindi un serbatoio da 50 litri, fatto di semplice lamiera o plastica, è in grado di trasportare 31 Nm3 di H2. Per poter trasportare lo stesso volume di H2 gassoso in un serbatoio a 200 bar questo ultimo dovrebbe avere una capacità di 155 litri, ed inoltre essere fatto di robuste pareti di alluminio perché l'acciaio diventerebbe fragile come vetro se messo a contatto con l'H2.
La suddetta capacità di stoccaggio di H2 dell'acido formico è vicina al limite minimo del 5,5% in peso stabilito dal Dipartimento dell'Energia degli Stati Uniti d'America per considerare efficienti le sostanze per lo stoccaggio di H2. L'acido formico potrebbe dunque giocare un ruolo di fondamentale importanza per facilitare lo stoccaggio e il trasporto dell'H2 negli usi pratici, a condizione di poter attuare facilmente la sua deidrogenazione.
Tale processo è stato ampiamente studiato e può essere ottenuto in modo relativamente semplice, sicuro e facilmente controllabile. La deidrogenazione dell'acido formico è una reazione che si può attuare mediante l'uso di appositi catalizzatori. Tuttavia, il problema pratico ancora da risolvere è trovare un catalizzatore di basso costo e alta selettività. La selettività è importante, perché altrimenti l'acido formico si decomporrebbe in CO (monossido di carbonio, tossico per inalazione) e acqua, rendendo quasi inutile l'utilizzo come vettore energetico perché il Potere Calorifico Inferiore (Pci) del CO è di solo 10 MJ/chilogrammo, contro i 120 MJ/chilogrammo dell'H2. I catalizzatori più efficienti, che consentono la scissione dell'acido formico in H2 e CO2, sono tutti a base di metalli rari quali iridio e palladio.
L'acido formico prodotto dalla biomassa
Indipendentemente dalla fattibilità tecnico economica di utilizzare l'acido formico come medio di trasporto dell'idrogeno, la grande domanda industriale di questo composto esige di trovare un'alternativa sostenibile all'attuale produzione da gas naturale. La biomassa rappresenta la più grande risorsa di carbonio al mondo ed è adatta per le sintesi chimiche.
Tra i diversi tipi di biomassa, la cellulosa si caratterizza per una composizione chimica adeguata - ha la giusta proporzione fra C, H e O - è poco costosa, facilmente disponibile ed è la più abbondante.
Le strategie di conversione della cellulosa finora esplorate (2) sono le seguenti:
- Idrolisi acida. Il trattamento della cellulosa o degli zuccheri con un acido forte, come ad esempio l'acido solforico, produce una serie di acidi organici. Il processo non è selettivo, per cui la percentuale di acido formico è piuttosto bassa, dell'ordine del 4%. La combinazione di un acido e un catalizzatore, ad esempio acido cloridrico e cloruro di cromo, raddoppia la resa in acido formico, ma ciò non basta a rendere il processo conveniente per finalità industriali.
- Ossidazione umida. Il trattamento della cellulosa con acqua a 400°C e 200 bar, eventualmente con aggiunta di ossigeno o perossido di idrogeno (acqua ossigenata), produce un cocktail di acidi organici ma, come nel caso precedente, non è un processo selettivo. L'aggiunta di idrossido di sodio (soda caustica) aumenta la resa in acido formico fino al 38% con solo 250°C. È possibile ottenere fino al 91% di acido formico mediante ossidazione del glucosio in una soluzione di acqua, perossido di idrogeno e una base adeguata (idrossido di litio, oppure di sodio, oppure di potassio). Questo apre la possibilità di produrre l'acido formico mediante un processo a due stadi: saccarificazione della biomassa cellulosica mediante trattamento enzimatico oppure acido e successivamente ossidazione umida del glucosio risultante.
- Ossidazione catalitica. L'ossidazione della cellulosa con ossigeno puro in presenza di un catalizzatore acido (vanadil solfato, VOSO4, oppure metavanadato di sodio, NaVO3) oppure di un catalizzatore eteropoliacido è in grado di produrre acido formico a temperature e pressioni basse o moderate. Con il primo catalizzatore il trattamento di paglia di frumento a 130°C e ossigeno puro a 30 bar ha prodotto il 47% di acido formico, valore che sale all'87% utilizzando glucosio anziché paglia. Da osservare che il 47% è una ottima resa, se consideriamo che la sostanza secca della paglia è composta da 35-39% di cellulosa e 23-30% di emicellulosa. Una resa del 47% di acido formico significa dunque un rendimento di conversione compreso fra il 72% e il 76%. Con il secondo catalizzatore, la resa massima ottenibile da biomassa vegetale è dell'ordine del 35%, che sale a 85% se il substrato è glucosio. Le condizioni di trattamento nel secondo caso sono state però meno severe: 78°C e ossigeno puro a 20 bar.
Leggi anche Bioetanolo da paglia, analisi dell'ennesimo fallimento
Nonostante negli ultimi dieci anni la conversione della biomassa in acido formico si sia sviluppata notevolmente, arrivando a processi con rese (teoricamente) accettabili, non esiste ancora un sistema integrato che soddisfi contemporaneamente tutti i requisiti per l'industrializzazione.
Sono stati sviluppati catalizzatori con alta efficienza e bassi costi energetici, ma questi possono presentare dei problemi di purificazione del prodotto, perché l'acido formico esce sotto forma di formiato (sale), il quale deve essere trattato ulteriormente. D'altro canto, i processi nei quali la separazione dell'acido formico è facile risultano in genere costosi ed energivori, oppure richiedono condizioni operative severe (alta pressione e/o temperatura) che si ripercuotono sul costo operativo e sulla sicurezza dell'impianto.
Non sembra dunque probabile che in un futuro immediato vengano sviluppati sistemi compatti e facilmente gestibili per la conversione delle biomasse in acido formico direttamente nelle aziende agricole.
Leggi anche Acido formico: la soluzione al problema dell'idrogeno? Seconda parte
Per maggiori approfondimenti
Lo stato dell'arte del bio-olio da pirolisi. Prima parte
Lo stato dell'arte del bio-olio da pirolisi. Seconda parte
La liquefazione idrotermica della biomassa
Bibliografia
(1) W.X. Chua, S. da Cunha, G.P. Rangaiah, K. Hidajat, Design and optimization of Kemira-Leonard process for formic acid production, Chemical Engineering Science: X, Volume 2, 2019, 100021, ISSN 2590-1400.
(2) Xi Chen, Ying Liu and Jingwei Wu, Sustainable production of formic acid from biomass and carbon dioxide Molecular Catalysis, Volume 483, March 2020, 110716; copia accessibile da questa pagina.