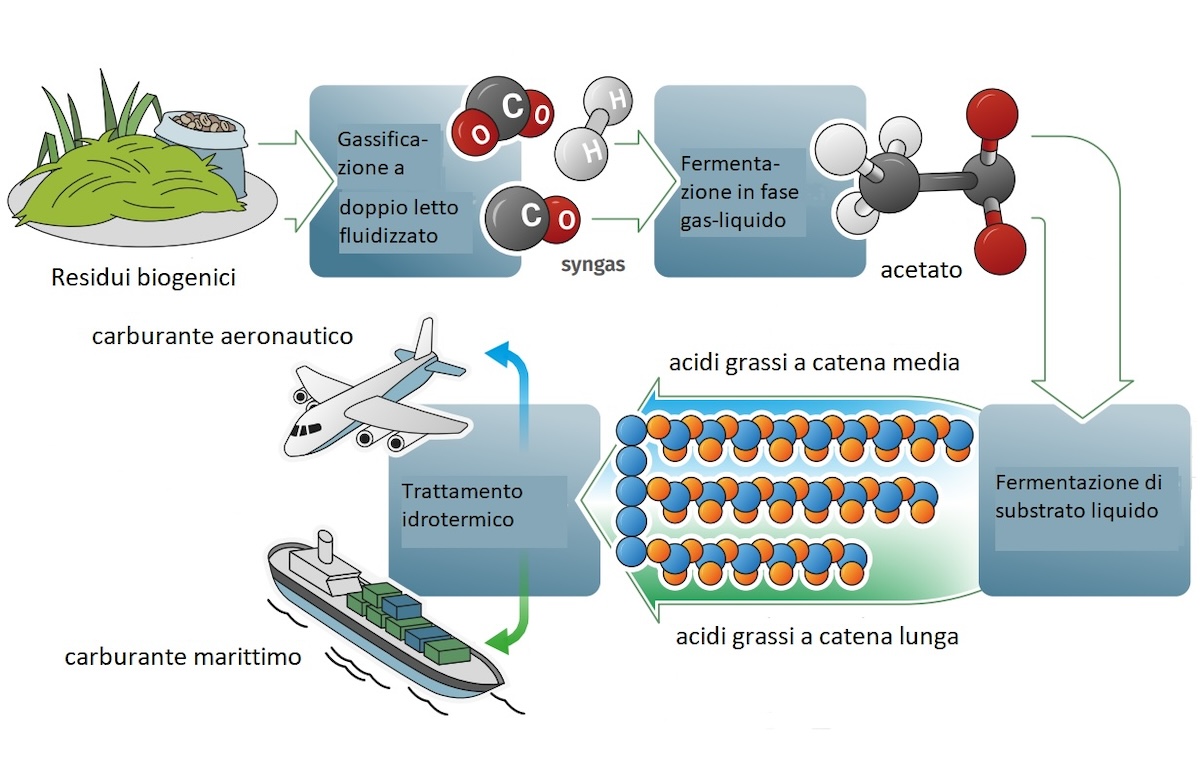
Il concetto di fermentazione gassosa è la generalizzazione delle tecnologie Power to gas e Syngas to methane, già trattate in precedenza. In estrema sintesi, l'idea consiste nel far gorgogliare una miscela di idrogeno, monossido di carbonio e diossido di carbonio in un medio di coltura di batteri acetogeni, i quali fungono da catalizzatori biologici e producono acido acetico, etanolo e altri composti chimici potenzialmente interessanti per l'industria. Il brodo di fermentazione andrebbe poi distillato per separare i prodotti dalla matrice acquosa.
I vantaggi di un tale approccio sulle tecnologie industriali come la sintesi Fischer-Tropsch consistono in un minore consumo energetico e in una semplicità operativa, in quanto i reattori lavorano a pressione quasi ambiente e a temperature sotto i 70°C. I batteri ammettono inoltre composizioni del gas variabili entro limiti più larghi e tenori di impurità più alti dei catalizzatori chimici. Ciò consente di sfruttare gas "sporchi" come il syngas senza bisogno di ricorrere a costosi sistemi di purificazione previ alla sintesi dei prodotti desiderati.
I prodotti più comuni della fermentazione gassosa sono l'acido acetico e l'etanolo, che possono essere utilizzati come prodotto chimico di base o come carburante. I composti di maggior valore per l'industria chimica sono però il butanolo e l'esanolo, i quali costituiscono lo scopo di ricerca del progetto tedesco Kopernikus P2X. Questi prodotti chimici organici di alto valore sono più versatili e vengono utilizzati, ad esempio, per la produzione di pitture, per la sintesi chimica come solventi o come combustibili. Attualmente, la produzione di questi prodotti chimici è principalmente basata sul petrolio, che è complesso, costoso e insostenibile a causa delle limitazioni dei vettori energetici fossili. Alcune specie di batteri acetogeni, ad esempio Clostridium carboxidivorans, sono in grado di produrre composti C4 e C6 (cioè con quattro e sei atomi di carbonio) direttamente dal syngas.
Un altro approccio noto in letteratura è la fermentazione in due fasi: i prodotti metabolici primari della fermentazione del syngas - acetato ed etanolo - vengono convertiti in un secondo fermentatore, ad esempio inoculato con Clostridium kluyveri, in composti a catena più lunga.
Un altro approccio ancora consiste nella coltura mista di due o più specie - ad esempio Clostridium autoethanogenum e Clostridium kluyveri - in un unico reattore, nel quale i composti C1 gassosi - CO e CO2 - possono essere convertiti microbicamente in composti C4 e C6 liquidi.
La fermentazione del gas di sintesi rappresenta una piattaforma molto promettente per la fissazione biotecnologica della CO2 nei prodotti chimici, ma ci sono ancora alcune sfide da superare. In particolare, le limitazioni causate dallo scarso trasferimento di massa gas-liquido a causa della bassa solubilità dei componenti del gas di sintesi, e le basse concentrazioni di cellule e prodotti nel brodo di fermentazione. Sebbene aziende operanti a livello globale come LanzaTech, INEOS Bio e Coskata Inc. già gestiscono (o hanno gestito) vari progetti dimostrativi - perlopiù fallimentari - sono essenziali ulteriori attività di ricerca e sviluppo.
L'attenzione si concentra sullo sviluppo di un biocatalizzatore potente e robusto, sull'ottimizzazione dei parametri di processo e sui miglioramenti del design del reattore in modo da ottenere un coefficiente di trasferimento di massa gas-liquido elevato. Non va sottovalutato il costo energetico di separazione dei prodotti, che si trovano molto diluiti in una grande massa di acqua, per cui è necessario mettere a punto tecnologie di concentrazione dei prodotti.
Il bioreattore come elemento centrale è cruciale per il successo nell'implementazione tecnica di un progetto biotecnologico. L'obiettivo principale è raggiungere un'elevata produttività volumetrica (chilogrammi di prodotto per volume del reattore e unità di tempo), ma tale obiettivo è legato alla concentrazione del biocatalizzatore (densità cellulare) e al flusso di CO e H2 nel brodo di fermentazione liquido, e da quest'ultimo alla cellula stessa. La progettazione del reattore e le condizioni operative dovrebbero pertanto favorire la massima funzionalità dei microrganismi, ma qui ci troviamo di fronte a requisiti contraddittori. In genere si riscontra che i batteri più efficienti sono quelli termofili (1), ma una temperatura operativa più alta comporta una minore solubilità dei gas (un principio fisico noto come Legge di Henry). Aumentare la solubilità del gas ad alte temperature richiede dunque di aumentare la pressione, ma ciò si traduce in un maggiore costo di fabbricazione del reattore (pareti più spesse) e di operazione (più energia per il pompaggio del medio di coltivazione e per la compressione del syngas). Nonostante gli evidenti svantaggi della fermentazione ad alta pressione, questa sembra essere la soluzione preferita da un gruppo di ricerca fiammingo, finanziato dall'Unione Europea (2).
Leggi anche La digestione anaerobica ad alta pressione
Oltre ai fermentatori ad alta pressione esistono almeno otto tecnologie diverse di reattori (3), ma quella che garantisce la maggiore efficienza di trasferimento del gas al medio liquido è il reattore a colonna di bollicine, a condizione che la colonna sia molto alta e sottile (design più complesso e maggiori perdite termiche dell'impianto) e le bollicine siano piccolissime (necessità di particolari membrane per costruire il gorgogliatore, maggiore pressione operativa del compressore, quindi maggiore consumo elettrico e sistemi di pulizia del syngas più accurati per evitare che le impurità tappino i pori delle membrane).
Secondo una ricerca pubblicata da Nature (4), la produzione di isopropanolo e acetone mediante fermentazione di syngas sarebbe un processo che addirittura fissa il carbonio anziché contribuire all'effetto serra. Detti composti sono gli ingredienti fondamentali per la produzione di solventi, per la fabbricazione di acrilico trasparente e di polipropilene, tutti prodotti industriali attualmente derivati dal petrolio per i quali non esistono processi di "chimica verde" competitivi. La produzione di bioacetone e biobutanolo è nota sin dai primi anni del Ventesimo Secolo, ma il processo ABE richiede zucchero o amido come materia prima, per cui è insostenibile. Il risultato ottenuto dai ricercatori statunitensi è però impossibile da replicare in Europa, perché basato su un microrganismo acetogeno geneticamente modificato per convertire syngas in acetone e isopropanolo.
La produttività massima di acetone, ottenuta con un reattore pilota da 150 litri, è stata di 1,8 grammi/litro.ora, con una selettività del 65%. Si intende per selettività la percentuale del carbonio contenuto nel syngas che viene effettivamente convertita nel prodotto desiderato. Nelle stesse condizioni, la produttività dell'isopropanolo è stata di 1,5 grammi/litro.ora, con una selettività del 75%. In tutti i casi, assieme all'acetone e all'isopropanolo si formano piccole quantità di acido acetico e di etanolo. Nel migliore dei casi sperimentati, circa il 5% del carbonio contenuto nel syngas si converte in biomassa batterica, aprendo la possibilità di produrre mangimi a base di proteine unicellulari.
La tecnologia della fermentazione gassosa è ancora agli esordi e difficilmente vedremo impianti nel breve termine. Ancora più difficilmente tali impianti saranno agricoli, almeno in Europa, perché sarà necessario rompere una serie di barriere ideologiche e politiche. Per prima cosa, sarebbe necessario che l'allevamento di batteri specifici e la produzione di ingredienti industriali come l'isopropanolo e l'acetone vengano riconosciuti come "attività agricola". Le massime produttività si possono raggiungere solo con organismi geneticamente modificati, cosa per ora vietatissima nell'Ue, per cui bisognerebbe accontentarsi di rendimenti molto più scarsi e quindi minore produttività rispetto ai concorrenti extracomunitari.
Lo studio (1 già citato) riflette l'ideologia imperante in Europa: l'inoculo per la fermentazione gassosa è stato prelevato da un impianto di biogas termofilo, alimentato con liquami suini e letame bovino, e successivamente adattato alla fermentazione di una miscela di CO2 - recuperata dal biogas - e H2. Nella visione dei ricercatori dell'Università Tecnica di Danimarca, lo scopo principale del processo è l'upgrading del biogas e l'acido acetico sarebbe solo un sottoprodotto che contribuisce a migliorare la redditività del sistema. Contrariamente al dogma europeo dell'idrogeno verde - prodotto mediante idrolisi dell'acqua, utilizzando eccedenti di energia fotovoltaica ed eolica - i ricercatori postulano l'utilizzo di H2 residuale, derivato dall'industria petrolchimica o dalla produzione di coke, fatto che però suona contraddittorio con l'implementazione di un tale processo in un impianto di biometano agricolo.
Nel concetto sviluppato dal progetto Biosfera esposto nell'immagine di apertura dell'articolo, il ruolo dell'agricoltura sarebbe semplicemente quello di conferire i residui colturali ad un impianto industriale. Una tale concezione di economia lineare è di dubbiosa sostenibilità perché andrebbe a sottrarre del prezioso carbonio organico ai suoli agricoli.
Bibliografia
(1) Basma Omar, Maie El-Gammal, Reda Abou-Shanab, Ioannis A. Fotidis, Irini Angelidaki, Yifeng Zhang, Biogas upgrading and biochemical production from gas fermentation: Impact of microbial community and gas composition, Bioresource Technology, Volume 286, 2019, 121413, ISSN 0960-8524.
(2) Wouter Van Hecke, Richard Bockrath, Heleen De Wever, Effects of moderately elevated pressure on gas fermentation processes, Bioresource Technology, Volume 293, 2019, 122129, ISSN 0960-8524.
(3) Stoll, I.K., Boukis, N. and Sauer, J. (2020), Syngas Fermentation to Alcohols: Reactor Technology and Application Perspective. Chemie Ingenieur Technik, 92: 125-136.
(4) Liew, F.E., Nogle, R., Abdalla, T. et al. Carbon-negative production of acetone and isopropanol by gas fermentation at industrial pilot scale. Nat Biotechnol 40, 335–344 (2022).