L'autore ha già espresso alcune perplessità sull'inefficienza termodinamica inerente il sistema proposto dagli ideologi di Bruxelles, documentate in un precedente articolo.
Idrogeno da biomasse e Green deal
Sono pochi i benefici che effettivamente potrebbe trarre l'Italia, e ancora meno quelli per le nostre aziende agricole. Nel caso estremo - molto improbabile - in cui l'idrogeno pulito dovesse sostituire il biometano, tutti gli investimenti delle aziende agroenergetiche fatti fino ad oggi andrebbero persi perché la domanda energetica verrebbe monopolizzata da grosse aziende e consorzi industriali. La corsa ai fondi europei per l'idrogeno pulito sembra che stia risvegliando l'interesse della ricerca per una tematica che sembrava ormai morta: quella del bioidrogeno. Se si dimostrasse la maggiore efficienza o almeno la convenienza economica della fermentazione oscura, fatto che per ora non si è mai verificato, sarebbe ipotizzabile convertire gli impianti di digestione anaerobica in impianti produttori di bioidrogeno.
Esploriamo in questo articolo quali sono le reali probabilità di un tale scenario.
Breve storia del bioidrogeno
Il bioidrogeno è una miscela di H2 e CO2 risultante da un processo anaerobico noto come dark fermentation, letteralmente "fermentazione oscura", chiamato così per differenziarlo da un altro processo fermentativo, la fotofermentazione (photofermentation). La fermentazione oscura è un processo molto simile alla digestione anaerobica, che avviene per l'attività di alcuni gruppi di batteri (fondamentalmente delle famiglie Clostridia, Enterobacter, Escherichia, Pseudomonas, Ruminococcus, Thermoanaerobacterium e Thermococcus, Rif. [i]). La giustificazione della ricerca sulla fermentazione oscura si basa sulla possibilità di rimpiazzare la classica digestione anaerobica, producendo idrogeno anziché metano, quindi energia senza emissioni di CO2 in atmosfera.L'argomento è un po' fallace perché in ogni caso le emissioni di CO2 causate dall'impiego del biometano non contano: esse sono "emissioni neutre", perché verranno riassorbite nel ciclo colturale successivo. Inoltre, la fermentazione anaerobica produce comunque CO2, in genere anche di più rispetto alla digestione anerobica. Una buona parte del carbonio contenuto nella biomassa viene trasformato in acido acetico, acido butirrico e altri acidi organici, butanolo e acetone. Se questi non vengono recuperati in qualche modo, andranno ulteriormente degradati dai batteri, producendo comunque CO2 ed eventualmente anche CH4.
A effetti puramente informativi, compariamo le stechiometrie della digestione anaerobica e della fermentazione oscura del glucosio.
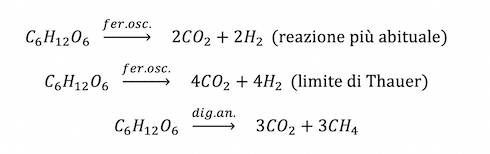
Osserviamo che, nel caso più favorevole in assoluto, noto come limite di Thauer, Rif. [ii], 180 grammi di glucosio rendono quattro moli di idrogeno, ovvero 0,0896 Nm3. Poiché il Pci (Potere calorifico inferiore) dell'H2 è pari a 3 kWh/Nm3, Rif. [iii], nel caso più favorevole si potrebbero ottenere 0,2688 kWh di energia termica. Con le migliori celle a idrogeno oggi disponibili, la cui reazione comunque emette vapore d'acqua, l'energia elettrica producibile è il 60% dell'energia termica, ovvero 0,161 kWh. Nel caso della digestione anaerobica, 180 grammi di glucosio rendono tre moli di metano, ovvero 0,0672 Nm3. Il Pci del CH4 è pari a 9,97 kWh/Nm3, Rif. [iii] già citato, quindi l'energia termica ottenuta è pari a 0,67 kWh. Il rendimento elettrico di un cogeneratore endotermico di buona qualità è del 42%, quindi l'energia elettrica ottenibile dalla digestione anaerobica di 180 grammi di glucosio è 0,281 kWh.
La maggiore efficienza energetica complessiva della digestione anaerobica, unita alla grande varietà di substrati che gli impianti convenzionali possono processare, spiega perché la produzione di energia mediante fermentazione oscura non ha avuto successo commerciale. L'argomento delle minori emissioni di CO2, con cui si giustificava anni fa l'interesse per la fermentazione oscura, non regge una semplice verifica termodinamica, neanche se si considerasse la CO2 biogenica imputabile al metano come "emissione di effetto serra". Si osservi che, nel migliore dei casi, la fermentazione oscura del glucosio rende 0,161 kWh ed emette 0,0896 Nm3 di CO2, prodotti dalla fermentazione stessa, ovvero 0,556 Nm3 CO2/kWh elettrico generato. Nel caso della digestione anaerobica del glucosio, la quantità totale di CO2 prodotta dalla combustione del CH4, più la CO2 risultante dal processo biologico, è pari a 0,134 Nm3, quindi l'ipotetica emissione specifica è 0,467 Nm3 CO2/kWh di energia elettrica.
Oltre il limite di Thauer
Un recente studio, condotto all'Università di Vienna e pubblicato dalla prestigiosa rivista scientifica Nature, Rif. [iv], afferma che è possibile oltrepassare il limite biologico riscontrato da Thauer nel lontano 1977. Come diceva il grande astronomo e divulgatore scientifico Carl Sagan, "Affermazioni straordinarie richiedono prove straordinarie": un principio che dovrebbe applicarsi nella revisione di pubblicazioni scientifiche, ma che spesso viene trascurato dai revisori.I ricercatori austriaci pomposamente affermano che: "Il nostro progetto di ingegnerizzazione di consorzi (batterici) potrebbe aprire la pista per lo sviluppo di una bioindustria della produzione di H2" (Our artificial consortia engineering blueprint might pave the way for the development of a H2 production bioindustry, Sic).
Stanno davvero così le cose? La metodologia utilizzata dagli austriaci per le loro prove biologiche è quella maggiormente in voga nella comunità scientifica centroeuropea, basata sulla norma VDI 4630, sulla quale l'autore ha già espresso non poche perplessità (si veda Focus critico sulla norma VDI 4630 I Parte e II Parte). Come di consueto, il paper non riporta un'analisi degli errori metrologici, ma possiamo stimare che questi difficilmente superino il 5%. L'incremento della produzione di H2 rispetto al limite di Thauer, ottenuto con una miscela di due popolazioni di batteri - Clostridium acetobutylicum (Foto 1) ed Enterobacter aerogenes - è risultato del 40%. Possiamo concedere il beneficio del dubbio e assumere che tale risultato sia vero e privo d'incertezza. La questione è: Può un aumento del 40% oltre il limite di Thauer giustificare "lo sviluppo di una bioindustira dell'H2"?
Facciamo una semplice verifica: stando allo studio in questione, 180 grammi di glucosio produrrebbero 0,125 Nm3 di H2, che nella logica del Green deal equivalgono a 0,225 kWh di energia elettrica generata con celle a combustibile. È certamente un progresso, ma di certo non costituisce "un'evidenza straordinaria" che dimostri l'affermazione dei ricercatori austriaci. Tale incremento della produzione di idrogeno è ancora insufficiente se comparato con gli 0,281 kWh di energia elettrica, che si potrebbero produrre mediante la semplice digestione anaerobica della stessa quantità di glucosio ed un generatore endotermico convenzionale. Inoltre, non dimentichiamo che la digestione anaerobica non richiede l'intervento di un biotecnologo per "fabbricare" un inoculo in grado di digerire efficientemente la maggioranza dei sottoprodotti e rifiuti organici: ci ha già pensato la natura nei milioni di anni di evoluzione dei ruminanti. E non dimentichiamo neanche che i motori endotermici ancora costano parecchio di meno rispetto alle celle di combustibile.

Foto 1: Colonia di Clostridium acetobutylicum in crescita su un substrato di cellulosa
(Crediti: David Ramey, Butanol, the other alternative fuel, DOI: 10.13140/RG.2.2.26006.04161)
Esiste un futuro per la fermentazione oscura?
In base ai semplici calcoli discussi sopra dovrebbe essere abbastanza chiaro per chiunque che l'evidenza sperimentale non supporta la tesi della produzione su larga scala di bioidrogeno a scopo puramente energetico.Alcune ricerche ridimensionano l'importanza della fermentazione scura, inserendola nel più ragionevole ruolo di processo unitario all'interno del concetto di bioraffineria. Citiamo ad esempio una tesi di laurea dell'Università di Parigi, la cui commissione include alcuni ricercatori italiani, Rif. [v].
Senza affermazioni trionfaliste ma con pragmatismo, la tesi in questione esplora alcune delle possibili applicazioni industriali della fermentazione oscura:
- La produzione di bioplastiche e di acidi organici, nel cui caso il bioidrogeno sarebbe un sottoprodotto, da consumare come vettore energetico all'interno del proprio processo.
- L'inserimento di uno stadio di fermentazione oscura all'interno di un impianto di digestione anaerobica, con lo scopo di ottenere biogas con un maggiore tenore di metano.
- L'impiego del digestato della fermentazione oscura come substrato per un processo di fotofermentazione. Tale approccio consentirebbe di ottenere rese di idrogeno interessanti, ma a scapito di una maggiore complessità impiantistica, che è difficile valutare a priori.
Ancora è presto per trarre conclusioni, ma almeno una cosa è certa: se ci sarà uno sviluppo dell'economia basata sull'idrogeno pulito, questo sarà per pura ideologia politica - o per favorire interessi di parte - e purtroppo a spese dei cittadini. La termodinamica non è un'opinione.
Bibliografia
[i] F. Cappa, Dark fermentation: aspetti microbiologici, Presentazione nel seminario "Innovazione tecnologica per il recupero di energia e risorse dai reflui agroindustriali", 5 ottobre 2015.[ii] Thauer, R. K., Jungermann, K., Decker, K., & Pi, P. P. H.--. (1977). Energy conservation in chemotrophic anaerobic bacteria. Bacteriological reviews, 41(3), 809.
[iii] Visita questa pagina.
[iv] Ergal, I., Gräf, O., Hasibar, B. et al. Biohydrogen production beyond the Thauer limit by precision design of artificial microbial consortia. Commun Biol 3, 443 (2020).
[v] Anish Ghimire, Dark fermentative biohydrogen production from organic waste and application of by-products in a biorefinery concept. Tesi dottore di ricerca in Tecnologie ambientali, 2015.





















